लेखक:
Lewis Jackson
निर्मितीची तारीख:
12 मे 2021
अद्यतन तारीख:
1 जुलै 2024

सामग्री
अणूमध्ये न्यूट्रॉनची संख्या निश्चित करणे अगदी सोपे आहे, आपल्याला कोणतेही प्रयोग करण्याची आवश्यकता नाही. सामान्य अणू किंवा समस्थानिकातील न्यूट्रॉनची संख्या काढण्यासाठी आपणास नियतकालिक सारणी तयार असणे आवश्यक आहे व त्या सूचनांचे अनुसरण करणे आवश्यक आहे.
पायर्या
पद्धत 1 पैकी 2: सामान्य अणूमध्ये न्यूट्रॉनची संख्या शोधा
नियतकालिक सारणीवरील घटकाची स्थिती निश्चित करा. उदाहरण म्हणून, आपल्याला वरुन सहाव्या ओळीत ओसमियम (ओस) हा घटक सापडेल.
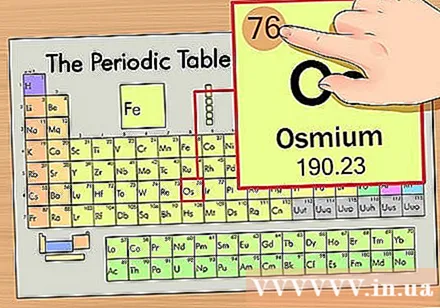
घटकाची अणु संख्या शोधा. ही सर्वात स्पष्ट संख्या आहे जी प्रत्येक घटकाद्वारे जाते आणि मुख्य चिन्हाच्या वर असते (ज्या बोर्डवर आम्ही वापरत आहोत तिथे इतर संख्या नाहीत). अणु संख्या ही त्या घटकाच्या एका अणूमधील प्रोटॉनची संख्या असते. ओस ही संख्या 76 76 आहे, ज्याचा अर्थ ऑसमियम अणूमध्ये prot 76 प्रोटॉन आहेत.- प्रोटॉनची संख्या कोणत्याही घटकामध्ये कधीही बदलत नाही; हे मूलत: एखाद्या घटकाचे वर्णन करण्याचे वैशिष्ट्य असते.
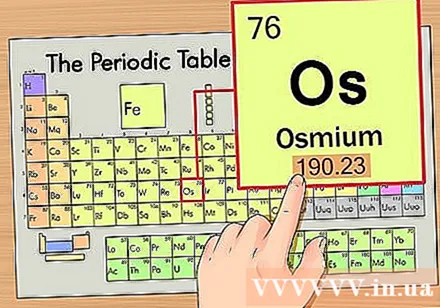
घटकाचे अणु वजन शोधा. ही संख्या सहसा मुख्य चिन्हाच्या खाली आढळते. लक्षात घ्या की या उदाहरणातील नियतकालिक सारणीत केवळ अणु क्रमांक आहे आणि अणूचा भार नाही. सर्व नियतकालिक सारण्या नाहीत. ओस्मियमचे अणु वजन 190.23 आहे.
अणू द्रव्य मिळविण्यासाठी अणूचे वजन सर्वात जवळच्या पूर्णांकात गोल करा. उदाहरणार्थ, १ 190 ०.२3 ची संख्या १ 190 ० पर्यंत होईल, तर ऑसमियमचा अणु द्रव्यमान १ 190 ० आहे.- अणू वजन समान रासायनिक घटकाच्या समस्थानिकेची सरासरी असते, म्हणूनच ते सहसा पूर्णांक नसते.
अणू द्रव्ये पासून अणु क्रमांक वजा करा. अणू द्रव्ये बहुतेक प्रोटॉन आणि न्यूट्रॉनचा वस्तुमान असल्यामुळे, अणू द्रव्यांमधून प्रोटॉनची संख्या वजा करतात (म्हणजे, अणु संख्या) मोजा अणूमध्ये न्यूट्रॉनची संख्या मिळवा. दशांश बिंदू नंतरची संख्या अणूमधील इलेक्ट्रॉनांच्या अगदी लहान जनतेचे प्रतिनिधित्व करते. या उदाहरणात, आमच्याकडे: 190 (मास अणू) - 76 (प्रोटॉनची संख्या) = 114 (न्यूट्रॉनची संख्या).
कृती लक्षात ठेवा. न्यूट्रॉनची संख्या शोधण्यासाठी, आम्ही फक्त खालील सूत्र लागू करतो: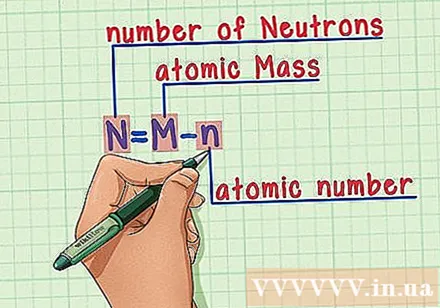
- एन = एम - एन
- एन = न्यूट्रॉनची संख्या
- एम = अणु द्रव्यमान
- एन = अणु संख्या
- एन = एम - एन
पद्धत २ पैकी: समस्थानिकातील न्यूट्रॉनची संख्या शोधा
नियतकालिक सारणीवरील घटकाची स्थिती निश्चित करा. उदाहरणार्थ कार्बन -१ is समस्थानिक घटक घेऊ. कार्बन -१ of चे समस्थानिक स्वरूप फक्त कार्बन (सी) असल्याने नियतकालिक टेबलवर कार्बन शोधा (वरून दुसरी पंक्ती).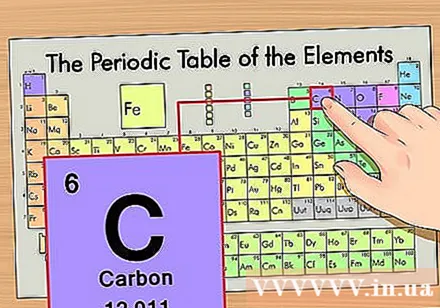
घटकाची अणु संख्या शोधा. ही सर्वात स्पष्ट संख्या आहे जी प्रत्येक घटकाद्वारे जाते आणि मुख्य चिन्हाच्या वर असते (ज्या बोर्डवर आम्ही वापरत आहोत तिथे इतर संख्या नाहीत). अणु संख्या ही त्या घटकाच्या एका अणूमधील प्रोटॉनची संख्या असते. सी क्रमांक 6 आहे, ज्याचा अर्थ कार्बन अणूमध्ये 6 प्रोटॉन आहेत.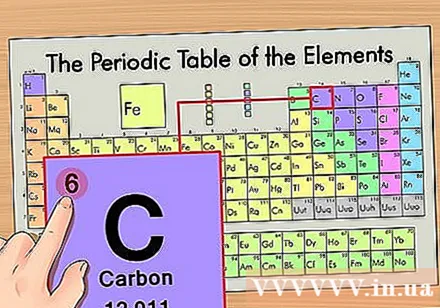
अणू वस्तुमान शोधा. आयसोटोप्ससह हे अत्यंत सोपे आहे कारण त्यांचे अणु द्रव्यमानाने नावे ठेवण्यात आली आहेत. उदाहरणार्थ, कार्बन -१ मध्ये १ of चे अणु द्रव्यमान असेल. एकदा तुम्हाला समस्थानिकेचा अणु द्रव्य सापडला तर न्युट्रॉनची संख्या शोधण्यासाठी उर्वरित चरण सामान्य अणूसारखेच असतील.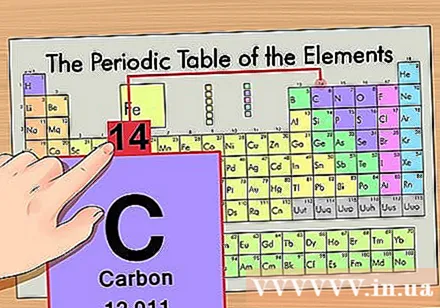
अणू द्रव्ये पासून अणु क्रमांक वजा करा. अणू द्रव्ये बहुतेक प्रोटॉन आणि न्यूट्रॉनचा वस्तुमान असल्यामुळे, अणू द्रव्यांमधून प्रोटॉनची संख्या वजा करतात (म्हणजे, अणु संख्या) मोजा अणूमध्ये न्यूट्रॉनची संख्या मिळवा. दशांश बिंदू नंतरची संख्या अणूमधील इलेक्ट्रॉनांच्या अगदी लहान जनतेचे प्रतिनिधित्व करते. या उदाहरणात, आपल्याकडेः 14 (मास अणू) - 6 (प्रोटॉनची संख्या) = 8 (न्यूट्रॉनची संख्या).
कृती लक्षात ठेवा. न्यूट्रॉनची संख्या शोधण्यासाठी आम्ही खालील सूत्र लागू करतो: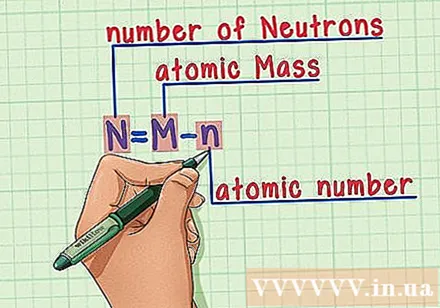
- एन = एम - एन
- एन = न्यूट्रॉनची संख्या
- एम = अणु द्रव्यमान
- एन = अणु संख्या
- एन = एम - एन
सल्ला
- एखाद्या घटकाचा वस्तुमान मोठ्या प्रमाणात प्रोटॉन आणि न्यूट्रॉनचा असतो, तर इलेक्ट्रॉन आणि इतर घटकांचा समूह नगण्य (शून्याच्या जवळ) असतो. प्रोटॉनचा वस्तुमान न्युट्रॉनच्या वस्तुमानाप्रमाणे असतो आणि अणु संख्या प्रोटॉनच्या संख्येचे प्रतिनिधित्व करते, म्हणून आम्ही एकूण वस्तुमानातून प्रोटॉनची संख्या सहजपणे वजा करतो.
- आपणास नियतकालिक सारणीवरील संख्येचा अर्थ आठवत नसेल तर लक्षात ठेवा नियतकालिक सारणी बहुतेक वेळा अणु संख्यांवर (म्हणजे प्रोटॉनची संख्या) तयार केली जाते, 1 (हायड्रोजन) पासून सुरू होते आणि त्यापासून एक युनिट वाढवते. डावीकडून उजवीकडे, 118 (ununoctium) ने समाप्त होणारी. प्रोटॉनची संख्या ही प्रत्येक अणूची ओळख पटणारी वैशिष्ट्ये असल्याने, ती सर्वात सोपी मालमत्ता आहे ज्यावर घटकांची व्यवस्था केली जाते. (उदाहरणार्थ, prot prot प्रोटॉन असलेले अणू नेहमीच सोन्याचे असतात म्हणून 2 प्रोटॉन असलेले अणू नेहमीच हीलियम असतात.)
स्रोत आणि उद्धरणे
- परस्परसंवादी नियतकालिक सारणी