लेखक:
Christy White
निर्मितीची तारीख:
8 मे 2021
अद्यतन तारीख:
1 जुलै 2024

सामग्री
- पाऊल टाकण्यासाठी
- 3 पैकी 1 पद्धत: भाग पहिला: इलेक्ट्रॉन शेल समजून घेणे
- 3 पैकी 2 पद्धत: भाग दोन: संक्रमणात धातू वगळता धातूंमध्ये व्हॅलेन्स इलेक्ट्रॉन शोधणे
- 3 पैकी 3 पद्धत: भाग तीन: ट्रान्झिशन मेटल्समध्ये व्हॅलेन्स इलेक्ट्रॉन शोधणे
- टिपा
- गरजा
व्हॅलेन्स इलेक्ट्रॉन घटकांच्या बाह्य शेलमध्ये असतात. अणूमधील व्हॅलेन्स इलेक्ट्रॉनची संख्या हा घटक तयार करू शकतो अशा प्रकारचे रासायनिक बंध निश्चित करते. घटकांची नियतकालिक सारणी वापरणे, व्हॅलेन्स इलेक्ट्रॉनची संख्या शोधण्याचा उत्तम मार्ग आहे.
पाऊल टाकण्यासाठी
3 पैकी 1 पद्धत: भाग पहिला: इलेक्ट्रॉन शेल समजून घेणे
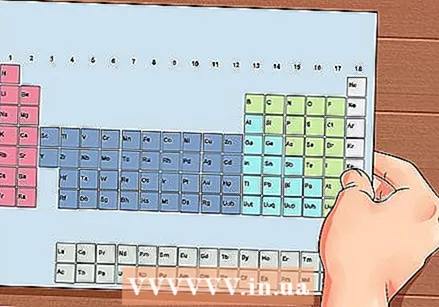 घटकांची नियतकालिक सारणी. हे रंग कोड असलेली एक सारणी आहे, जिथे प्रत्येक कक्षात एक घटक अणु क्रमांक आणि 1 ते 3 अक्षरे चिन्ह म्हणून दर्शविला जातो.
घटकांची नियतकालिक सारणी. हे रंग कोड असलेली एक सारणी आहे, जिथे प्रत्येक कक्षात एक घटक अणु क्रमांक आणि 1 ते 3 अक्षरे चिन्ह म्हणून दर्शविला जातो. 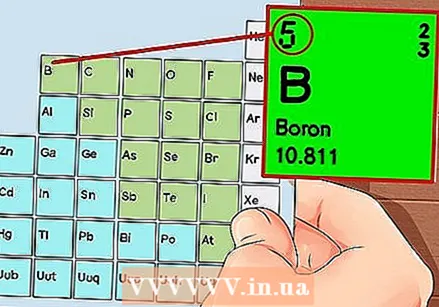 घटकाची अणु संख्या शोधा. अणूची संख्या घटकाच्या चिन्हाच्या वर किंवा पुढे आहे. उदाहरणार्थ: बोरॉन (बी) मध्ये अणूची संख्या 5 आहे, ज्याचा अर्थ असा आहे की यात 5 प्रोटॉन आणि 5 इलेक्ट्रॉन आहेत.
घटकाची अणु संख्या शोधा. अणूची संख्या घटकाच्या चिन्हाच्या वर किंवा पुढे आहे. उदाहरणार्थ: बोरॉन (बी) मध्ये अणूची संख्या 5 आहे, ज्याचा अर्थ असा आहे की यात 5 प्रोटॉन आणि 5 इलेक्ट्रॉन आहेत. 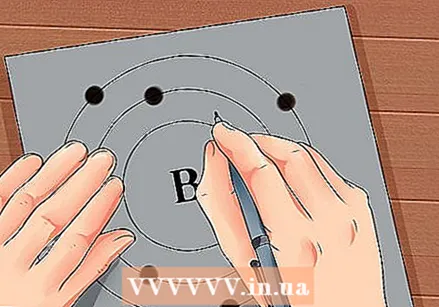 अणूचे साधे प्रतिनिधित्व काढा आणि इलेक्ट्रॉनच्या मध्यभागी कक्षाच्या मध्यभागी इलेक्ट्रॉन ठेवा. या नोक्यांना शेल किंवा ऊर्जा पातळी देखील म्हणतात. एकाच शेलमध्ये असू शकतात अशा इलेक्ट्रॉनची जास्तीत जास्त संख्या निश्चित केली जाते, आणि शेल आतील ते बाह्य कक्षापर्यंत भरले जातात.
अणूचे साधे प्रतिनिधित्व काढा आणि इलेक्ट्रॉनच्या मध्यभागी कक्षाच्या मध्यभागी इलेक्ट्रॉन ठेवा. या नोक्यांना शेल किंवा ऊर्जा पातळी देखील म्हणतात. एकाच शेलमध्ये असू शकतात अशा इलेक्ट्रॉनची जास्तीत जास्त संख्या निश्चित केली जाते, आणि शेल आतील ते बाह्य कक्षापर्यंत भरले जातात. - के शेल (अंतर्गत): 2 इलेक्ट्रॉन जास्तीत जास्त.
- एल शेल: जास्तीत जास्त 8 इलेक्ट्रॉन.
- एम शेल: जास्तीत जास्त 18 इलेक्ट्रॉन.
- एन शेल: जास्तीत जास्त 32 इलेक्ट्रॉन.
- ओ शेल: जास्तीत जास्त 50 इलेक्ट्रॉन.
- पी शेल (बाह्य): 72 इलेक्ट्रॉन जास्तीत जास्त.
 बाह्य शेलमध्ये इलेक्ट्रॉनची संख्या शोधा. हे व्हॅलेन्स इलेक्ट्रॉन आहेत.
बाह्य शेलमध्ये इलेक्ट्रॉनची संख्या शोधा. हे व्हॅलेन्स इलेक्ट्रॉन आहेत. - जेव्हा व्हॅलेन्स शेल भरलेले असते तेव्हा घटक स्थिर असतो.
- जर व्हॅलेन्स शेल भरलेला नसेल तर तो घटक रिअॅक्टिव्ह आहे, ज्याचा अर्थ असा आहे की तो रासायनिकरित्या दुसर्या घटकाच्या अणूशी बंधन घालू शकतो. प्रत्येक अणू व्हॅलेन्स शेल पूर्ण भरण्याच्या प्रयत्नात आपले व्हॅलेन्स इलेक्ट्रॉन सामायिक करतो.
3 पैकी 2 पद्धत: भाग दोन: संक्रमणात धातू वगळता धातूंमध्ये व्हॅलेन्स इलेक्ट्रॉन शोधणे
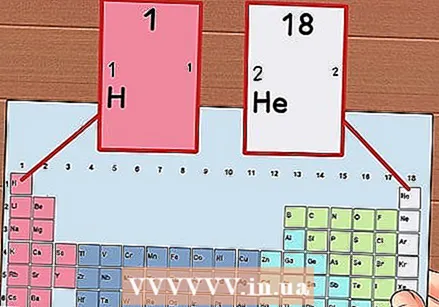 1 ते 18 पर्यंत नियतकालिक सारणीच्या प्रत्येक स्तंभची संख्या करा. हायड्रोजन (एच) स्तंभ 1 च्या शीर्षस्थानी आहे आणि स्तंभ 18 च्या शीर्षस्थानी हेलियम (तो) आहे. हे घटकांचे भिन्न गट आहेत.
1 ते 18 पर्यंत नियतकालिक सारणीच्या प्रत्येक स्तंभची संख्या करा. हायड्रोजन (एच) स्तंभ 1 च्या शीर्षस्थानी आहे आणि स्तंभ 18 च्या शीर्षस्थानी हेलियम (तो) आहे. हे घटकांचे भिन्न गट आहेत. 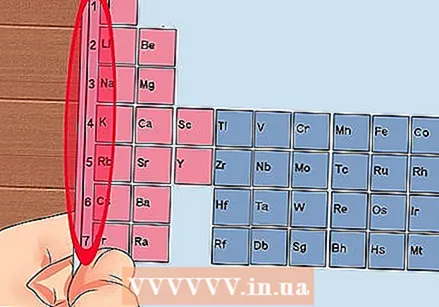 1 ते 7 पर्यंत प्रत्येक पंक्तीस एक नंबर द्या. हे घटकांचे पूर्णविराम असतात आणि ते अणूच्या कवच किंवा ऊर्जेच्या पातळीशी संबंधित असतात.
1 ते 7 पर्यंत प्रत्येक पंक्तीस एक नंबर द्या. हे घटकांचे पूर्णविराम असतात आणि ते अणूच्या कवच किंवा ऊर्जेच्या पातळीशी संबंधित असतात. - हायड्रोजन (एच) आणि हेलियम (तो) या दोहोंचे 1 शेल आहेत, तर फ्रान्सियम (एफआर) चे 7 आहेत.
- लॅन्थेनाइड्स आणि अॅक्टिनसाइड्स गटबद्ध आणि मुख्य सारणीच्या खाली सूचीबद्ध आहेत. सर्व लॅन्थेनाईड्स पीरियड 6, ग्रुप 3 आणि सर्व अॅक्टिनाइड्स पीरियड 7, ग्रुप 3 मधील आहेत.
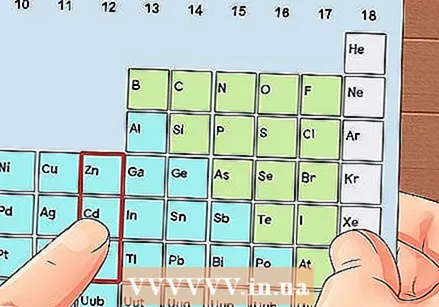 संक्रमण धातु नसलेले घटक शोधा. संक्रमण धातू 3 ते 12 च्या गटात असतात. इतर धातूंचे गट क्रमांक व्हॅलेन्स इलेक्ट्रॉनची संख्या दर्शवितात.
संक्रमण धातु नसलेले घटक शोधा. संक्रमण धातू 3 ते 12 च्या गटात असतात. इतर धातूंचे गट क्रमांक व्हॅलेन्स इलेक्ट्रॉनची संख्या दर्शवितात. - गट 1: 1 व्हॅलेन्स इलेक्ट्रॉन
- गट 2: 2 व्हॅलेन्स इलेक्ट्रॉन
- गट 13: 3 व्हॅलेन्स इलेक्ट्रॉन
- गट 14: 4 व्हॅलेन्स इलेक्ट्रॉन
- गट 15: 5 व्हॅलेन्स इलेक्ट्रॉन
- गट 16: 6 व्हॅलेन्स इलेक्ट्रॉन
- गट 17: 7 व्हॅलेन्स इलेक्ट्रॉन
- गट 18: 8 व्हॅलेन्स इलेक्ट्रॉन - हेलियम वगळता, ज्यात 2 आहेत
3 पैकी 3 पद्धत: भाग तीन: ट्रान्झिशन मेटल्समध्ये व्हॅलेन्स इलेक्ट्रॉन शोधणे
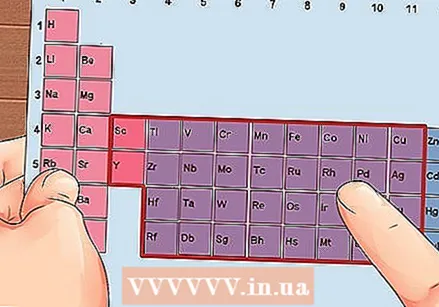 गट 3 ते 12 मधील घटक, संक्रमण धातू शोधा.
गट 3 ते 12 मधील घटक, संक्रमण धातू शोधा. गट संख्येवर आधारित व्हॅलेन्स इलेक्ट्रॉनची संख्या निश्चित करा. हे गट क्रमांक व्हॅलेन्स इलेक्ट्रॉनच्या संभाव्य संख्येशी संबंधित आहेत.
गट संख्येवर आधारित व्हॅलेन्स इलेक्ट्रॉनची संख्या निश्चित करा. हे गट क्रमांक व्हॅलेन्स इलेक्ट्रॉनच्या संभाव्य संख्येशी संबंधित आहेत. - गट 3: 3 व्हॅलेन्स इलेक्ट्रॉन
- गट 4: 2 ते 4 व्हॅलेन्स इलेक्ट्रॉन
- गट 5: 2 ते 5 व्हॅलेन्स इलेक्ट्रॉन
- गट 6: 2 ते 6 व्हॅलेन्स इलेक्ट्रॉन
- गट 7: 2 ते 7 व्हॅलेन्स इलेक्ट्रॉन
- गट 8: 2 किंवा 3 व्हॅलेन्स इलेक्ट्रॉन
- गट 9: 2 किंवा 3 व्हॅलेन्स इलेक्ट्रॉन
- गट 10: 2 किंवा 3 व्हॅलेन्स इलेक्ट्रॉन
- गट 11: 1 किंवा 2 व्हॅलेन्स इलेक्ट्रॉन
- गट 12: 2 व्हॅलेन्स इलेक्ट्रॉन
टिपा
- संक्रमण धातुंमध्ये व्हॅलेन्स शेल असू शकतात जे पूर्णपणे भरलेले नाहीत. संक्रमण धातुंमध्ये व्हॅलेन्स इलेक्ट्रॉनची नेमकी संख्या निश्चित करण्यासाठी क्वांटम सिद्धांताची काही तत्त्वे आवश्यक आहेत जी या कागदाच्या व्याप्तीच्या बाहेर आहेत.
गरजा
- घटकांची नियतकालिक सारणी
- पेन्सिल
- कागद