लेखक:
Monica Porter
निर्मितीची तारीख:
17 मार्च 2021
अद्यतन तारीख:
1 जुलै 2024

सामग्री
मोलर एकाग्रता विद्राव्य द्रवाची संख्या आणि द्रावणाची मात्रा यांच्यातील संबंध दर्शवते. मोलारिटीची गणना करण्यासाठी, आपण मोल्स आणि व्हॉल्यूम, वस्तुमान आणि व्हॉल्यूम किंवा मोल्स आणि मिलीलीटर (मिली) सह प्रारंभ करू शकता. त्यानंतर, वरील व्हेरिएबल्ससह, योग्य परिणाम मिळविण्यासाठी मूलक दाढीची एकाग्रता फॉर्म्युला लागू करा.
पायर्या
4 पैकी 1 पद्धत: मोलर क्रमांक आणि व्हॉल्यूममधून मोल एकाग्रतेची गणना करा
दाढीच्या एकाग्रतेची गणना करण्यासाठी मूलभूत सूत्र जाणून घेणे महत्वाचे आहे. लिटरमध्ये द्रावणाची मात्रा विभाजित करुन विरघळणार्या मोल्सच्या संख्येइतकी मोलर एकाग्रता. तेथून आमच्याकडे खालील सूत्र आहे: मॉलर एकाग्रता = विरघळणार्या मोल्सची संख्या / द्रावण लिटरची संख्या
- उदाहरणः 2.२ लिटर द्रावणामध्ये एनएसीएलच्या ०.7575 मोल्स असलेल्या सोल्यूशनची मोलार एकाग्रता काय आहे?

विषयाचे विश्लेषण करा. मोलारच्या एकाग्रतेची गणना करण्यासाठी आपल्याला लिटरमध्ये मोल्सची संख्या आणि द्रावणाची मात्रा आवश्यक आहे. दिलेल्या विषयामुळे आपल्याला या दोन मूल्यांची गणना करण्याची आवश्यकता नाही.- उदाहरणार्थ:
- मोलची संख्या = एनएसीएलच्या 0.75 मोल्स
- खंड = 4.2 एल
- उदाहरणार्थ:
खंडानुसार मोल्सची संख्या विभाजित करा. व्हॉल्यूमनुसार तीळ विभाजनाचा परिणाम म्हणजे द्रावणासाठी प्रति लिटर मोल्सची संख्या किंवा त्या द्रावणाची दाढी एकाग्रता.
- उदाहरणः दाढर एकाग्रता = विरघळलेल्या मोल्सची संख्या / द्रावण लिटरची संख्या = 0.75 मोल / 4..२ एल = ०.7785857१14२

आपले निकाल नोंदवा. स्वल्पविरामा नंतर दोन किंवा तीन संख्येची गोल, शिक्षकांच्या विनंतीनुसार किंवा असाइनमेंटवर अवलंबून. आपले परिणाम रेकॉर्ड करताना, "मोलार एकाग्रता" "एम" सह संक्षेप करा आणि विरघळणारे रासायनिक चिन्ह समाविष्ट करा.- उदाहरणार्थ: 0.179 एम NaCl
4 पैकी 2 पद्धत: मास आणि व्हॉल्यूममधून मोल एकाग्रतेची गणना करा
दाढीच्या एकाग्रतेची गणना करण्यासाठी मूलभूत सूत्र माहित असणे आवश्यक आहे. मोलर एकाग्रता विद्राव्य द्रवाची संख्या आणि द्रावणाची मात्रा यांच्यातील संबंध दर्शवते. दाढीच्या एकाग्रतेची गणना करण्याचे सूत्र खालीलप्रमाणे आहे. दाल एकाग्रता = विरघळली जाणे / समाधान लिटर संख्या
- समस्येचे उदाहरणः केएमएनओचे 3,4 ग्रॅम विरघळल्यानंतर सोल्यूशनच्या मोलची संख्या मोजा4 5.2 लिटर पाण्यात.

विषयाचे विश्लेषण कराः दाढीची एकाग्रता शोधण्यासाठी आपल्याला लिटरमध्ये मोल्सची संख्या आणि द्रावणाची मात्रा आवश्यक आहे. जर ही मूल्ये दिली गेली नाहीत परंतु सोल्यूशनची मात्रा आणि वस्तुमान आपल्याला माहिती असेल तर आपण दाढीच्या एकाग्रतेची गणना करण्यापूर्वी विद्राव्य मॉल्सची संख्या निश्चित करू शकता.- उदाहरणार्थ:
- वजन = 3.4 ग्रॅम केएमएनओ4
- खंड = 5.2 एल
- उदाहरणार्थ:
विद्राव्य द्रव्यमान रेणूची गणना करा. त्या द्रव्य किंवा ग्रॅममधून विरघळणार्या विद्रावाची संख्या मोजण्यासाठी आपल्याला प्रथम विद्राव्य द्रव्यमान रेणू निश्चित करणे आवश्यक आहे. द्रावणामध्ये प्रत्येक घटकाचे वस्तुमान अणू जोडून विद्राव्य द्रव्यमान रेणू निश्चित केले जाऊ शकते. प्रत्येक घटकाचे क्यूबिक अणू शोधण्यासाठी घटकांच्या नियतकालिक सारणीचा वापर करा.
- उदाहरणार्थ:
- के मासचे अणू = 39.1 ग्रॅम
- Mn चे मास अणू = 54,9 ग्रॅम
- ओ चे मास अणू = 16,0 ग्रॅम
- वस्तुमानाचे एकूण अणू = के + एमएन + ओ + ओ + ओ + ओ = 39.1 + 54.9 + 16 + 16 + 16 + 16 = 158.0 ग्रॅम
- उदाहरणार्थ:
मोलमध्ये ग्रॅम रुपांतरित करा. एकदा आपल्याकडे मोलार द्रव्यमान झाल्यानंतर, आपण द्रावणामध्ये ग्रॅम विरघळल्या जाणा .्या विरघळाच्या तुलनेत 1 मोल प्रति मोलार समकक्ष रूपांतर घटकाद्वारे गुणाकार करणे आवश्यक आहे. या गुणाकाराचा परिणाम म्हणजे विद्राव्य द्रव्याची संख्या.
- उदाहरणः विरघळलेला ग्रॅम * (1 / द्रावणातील द्राक्षे द्रव्यमान) = 3.4 ग्रॅम * (1 मोल / 158 ग्रॅम) = 0.0215 मोल
लिटरच्या संख्येने मोल्सची संख्या विभाजित करा. आता आपण मोल्सची संख्या मोजली आहे, आता त्या संख्येचे प्रमाण लिटरमध्ये विभाजित करा, आपल्याला त्या द्रावणाची दाब एकाग्रता मिळेल.
- उदाहरणः मोलार एकाग्रता = विरघळलेल्या मोल्सची संख्या / द्रावण लिटरची संख्या = 0.0215 मोल / 5.2 एल = 0.004134615
आपले निकाल नोंदवा. आपल्याला शिक्षकांनी आवश्यकतेनुसार निकाल गोळा करणे आवश्यक आहे, सहसा स्वल्पविरामानंतर दोन ते तीन संख्या. याव्यतिरिक्त, निकाल लिहिताना, "मोलार एकाग्रता" ला "एम" म्हणून संक्षिप्त करा आणि सोल्यूटचे रासायनिक प्रतीक सोबत घ्या.
- उदाहरणार्थ: 0.004 एम केएमएनओ4
कृती 3 पैकी 3: सोल्यूशनच्या सोल्यूशन्स आणि सोलिलिटर्सच्या संख्येमधून मोलर एकाग्रतेची गणना करा
दाढीच्या एकाग्रतेचे सूत्र माहित असणे आवश्यक आहे. मोलार एकाग्रतेची गणना करण्यासाठी. सोल्यूशनच्या मिलीलीटरने नव्हे तर आपल्याला सोल्यूशन प्रति लिटर विरघळलेल्या मोल्सची गणना करणे आवश्यक आहे. दाढीच्या एकाग्रतेची गणना करण्याचे सामान्य सूत्र असे आहे: दाल एकाग्रता = विरघळलेल्या मोल्सची संख्या / द्रावण लिटरची संख्या
- उदाहरणः CaCl चे 1.2 मोल्स असलेल्या सोल्यूशनच्या मोलार एकाग्रतेची गणना करा2 2905 मिलीलीटर पाण्यात.
विषयाचे विश्लेषण करा. मोलारच्या एकाग्रतेची गणना करण्यासाठी आपल्याला विरघळलेल्या मॉल्सची संख्या आणि लिटरमध्ये द्रावणाची मात्रा आवश्यक आहे. जर मिलीलीटरमध्ये समस्येमध्ये द्रावणाची मात्रा दिली गेली असेल तर गणना करण्यापूर्वी लिटरमध्ये समतुल्य व्हॉल्यूममध्ये रूपांतरित करा.
- उदाहरणार्थ:
- मोलची संख्या = सीएसीएलचे 1.2 मोल2
- खंड = 2905 मिली
- उदाहरणार्थ:
मिलीलीटरला लिटरमध्ये रुपांतरित करा. द्रावणास मिलीलीटरपासून लिटरमध्ये रुपांतरित करण्यासाठी, मिलीलीटरची संख्या 1000 ने विभाजित करा, कारण प्रत्येक लिटर 1000 मिलीलीटरच्या बरोबरीचे आहे. दशांश बिंदू 3 अंक बाकी सोडवून आपण मिलीलिटरला लिटरमध्ये रूपांतरित देखील करू शकता.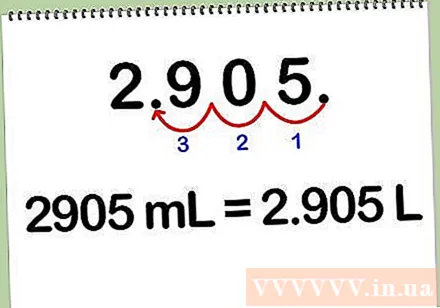
- उदाहरणार्थ: 2905 मिली * (1 एल / 1000 मिली) = 2,905 एल
लिटरच्या संख्येने मोल्सची संख्या विभाजित करा. आपल्याकडे लिटरची संख्या झाल्यानंतर, आपण मोलची संख्या लिटर सोल्यूशनच्या संख्येने विभाजित करून मोलारच्या एकाग्रतेची गणना करू शकता.
- उदाहरणः मोलार एकाग्रता = विरघळलेल्या मोल्सची संख्या / द्रावण लिटरची संख्या = सीएसीएलच्या 1.2 मोल2 / 2,905 एल = 0.413080895
आपले निकाल नोंदवा. दोन किंवा तीन स्वल्पविरामांकरिता निकाल आपल्या शिक्षकांद्वारे विनंती केल्याप्रमाणे लक्षात ठेवा. निकाल रेकॉर्ड करताना, "दाढीची एकाग्रता" "एम" म्हणून संक्षिप्त करा आणि नंतर विरघळण्यासाठीचे रासायनिक चिन्ह.
- उदाहरणार्थ: 0.413 एम CaCl2
4 पैकी 4 पद्धत: अतिरिक्त सराव
जेव्हा 5.2 ग्रॅम एनएसीएल 800 मिली पाण्यात विरघळली जाते तेव्हा सोल्यूशनच्या मोलार एकाग्रतेची गणना करा. समस्येद्वारे दिलेली मूल्ये ठरवा: ग्रॅममध्ये वस्तुमान आणि मिलीलीटरमध्ये व्हॉल्यूम.
- मास = 5.2 ग्रॅम एनएसीएल
- खंड = 800 मिली पाणी
ना घटकाचे क्यूबिक अणू आणि Cl चा घन अणू जोडून NaCl चे द्रव्य रेणू शोधा.
- नाचे मास अणू = 22.99 ग्रॅम
- सीएलचे मास अणू = 35.45 ग्रॅम
- NaCl = 22.99 + 35.45 = 58.44 ग्रॅमचे वस्तुमान रेणू
दाल रूपांतरण घटकाद्वारे विद्राव्य द्रव्यमानाचा गुणाकार करा. या उदाहरणात, NaCl चे आण्विक द्रव्यमान 58.44 g आहे, त्यामुळे रूपांतरण घटक "1 मोल / 58.44 ग्रॅम" आहे.
- एनएसीएल तीळची संख्या = 5.2 ग्रॅम एनएसीएल * (1 मोल / 58.44 ग्रॅम) = 0.8898 मोल = 0.09 मोल
800 मिली पाण्यात 1000 ने विभागून घ्या, आपल्याला लिटरमध्ये पाण्याचे प्रमाण मिळेल.
- आपण मिलीलीटरपासून लिटरमध्ये 1 एल / 1000 मिली रूपांतरण घटकाद्वारे 800 मिली देखील गुणाकार करू शकता.
- वरील प्रमाणे गुणाकार प्रक्रिया लहान करण्यासाठी आपण दशांश बिंदू 3 अंक डावीकडे परत करू शकता.
- खंड = 800 मिली 800 * (1 एल / 1000 मिली) = 800 मिली / 1000 मिली = 0.8 एल
लिटरमध्ये सोल्यूशनच्या व्हॉल्यूमद्वारे विद्रव्य च्या मोल्सची संख्या विभाजित करा. मोलारच्या एकाग्रतेची गणना करण्यासाठी आपल्याला लिटरमध्ये द्रावणाची मात्रा करून विरघळणारे 0.09 मोल (या प्रकरणात, एनएसीएल) विभाजित करणे आवश्यक आहे.
- मॉलर एकाग्रता = विरघळणार्या मोल्सची संख्या / द्रावण लिटरची संख्या = ०.० m मोल / ०. L एल = ०.११२5 मोल / एल
अंतिम निकाल नोंदवा. स्वल्पविरामानंतर निकालाला दोन किंवा तीन अंकी गोल करा आणि विद्रव्य रासायनिक चिन्हासह "एम" सह "दाढी एकाग्रता" ला संक्षिप्त करा.
- निकाल: 0.11 एम एनएसीएल