लेखक:
Sara Rhodes
निर्मितीची तारीख:
12 फेब्रुवारी 2021
अद्यतन तारीख:
1 जुलै 2024

सामग्री
- पावले
- 2 पैकी 1 भाग: रसायनशास्त्राच्या नियमांनुसार ऑक्सिडेशन अवस्थेचे निर्धारण
- भाग 2 मधील 2: रसायनशास्त्राचे नियम न वापरता ऑक्सिडेशन स्थिती निश्चित करणे
- टिपा
- आपल्याला काय आवश्यक आहे
रसायनशास्त्रात, "ऑक्सिडेशन" आणि "कमी" या शब्दाचा अर्थ असा होतो की ज्यामध्ये अणू किंवा अणूंचा समूह अनुक्रमे गमावतो किंवा इलेक्ट्रॉन मिळवतो. ऑक्सिडेशन स्टेट हे एक किंवा अधिक अणूंना नियुक्त केलेले संख्यात्मक मूल्य आहे जे पुनर्वितरित इलेक्ट्रॉनची संख्या दर्शवते आणि प्रतिक्रिया दरम्यान हे इलेक्ट्रॉन अणूंमध्ये कसे वितरीत केले जातात हे दर्शविते. या मूल्याचे निर्धारण ही अणू आणि त्यामध्ये असलेल्या रेणूंवर अवलंबून साधी आणि बरीच जटिल प्रक्रिया असू शकते. शिवाय, काही घटकांच्या अणूंमध्ये अनेक ऑक्सिडेशन अवस्था असू शकतात. सुदैवाने, ऑक्सिडेशन स्थिती निश्चित करण्यासाठी साधे अस्पष्ट नियम आहेत, ज्याचा आत्मविश्वासाने वापर करण्यासाठी रसायनशास्त्र आणि बीजगणित मूलभूत गोष्टी जाणून घेणे पुरेसे आहे.
पावले
2 पैकी 1 भाग: रसायनशास्त्राच्या नियमांनुसार ऑक्सिडेशन अवस्थेचे निर्धारण
 1 प्रश्नातील पदार्थ मूलभूत आहे का ते ठरवा. रासायनिक संयुगाच्या बाहेर अणूंची ऑक्सिडेशन स्थिती शून्य आहे. हा नियम स्वतंत्र मुक्त अणूंपासून तयार होणाऱ्या पदार्थांसाठी आणि ज्यात दोन, किंवा एका मूलद्रव्याचे पॉलिआटोमिक रेणू असतात त्यांच्यासाठी खरे आहे.
1 प्रश्नातील पदार्थ मूलभूत आहे का ते ठरवा. रासायनिक संयुगाच्या बाहेर अणूंची ऑक्सिडेशन स्थिती शून्य आहे. हा नियम स्वतंत्र मुक्त अणूंपासून तयार होणाऱ्या पदार्थांसाठी आणि ज्यात दोन, किंवा एका मूलद्रव्याचे पॉलिआटोमिक रेणू असतात त्यांच्यासाठी खरे आहे. - उदाहरणार्थ, अल(चे) आणि Cl2 0 ची ऑक्सिडेशन स्थिती आहे, कारण दोन्ही रासायनिक अनबाउंड मूलभूत अवस्थेत आहेत.
- लक्षात घ्या की सल्फर एस चे अॅलोट्रॉपिक रूप8, किंवा ऑक्टासेरा, त्याच्या atypical रचना असूनही, देखील एक शून्य ऑक्सिडेशन स्थिती द्वारे दर्शविले जाते.
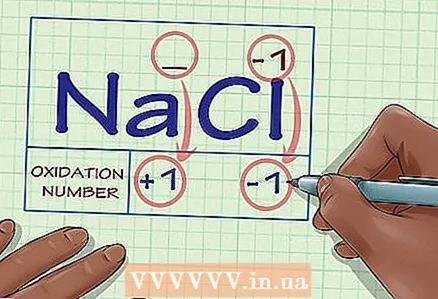 2 प्रश्नातील पदार्थ आयनांनी बनलेला आहे का ते ठरवा. आयनांची ऑक्सिडेशन स्थिती त्यांच्या शुल्काच्या बरोबरीची आहे. हे विनामूल्य आयन आणि रासायनिक संयुगेचा भाग असलेल्यांसाठी खरे आहे.
2 प्रश्नातील पदार्थ आयनांनी बनलेला आहे का ते ठरवा. आयनांची ऑक्सिडेशन स्थिती त्यांच्या शुल्काच्या बरोबरीची आहे. हे विनामूल्य आयन आणि रासायनिक संयुगेचा भाग असलेल्यांसाठी खरे आहे. - उदाहरणार्थ, Cl ion ची ऑक्सिडेशन अवस्था -1 आहे.
- रासायनिक संयुग NaCl मधील Cl ion ची ऑक्सिडेशन स्थिती देखील -1 आहे. व्याख्येनुसार ना आयनचा +1 चा चार्ज असल्याने, आम्ही निष्कर्ष काढतो की Cl आयनचा चार्ज -1 आहे, आणि अशा प्रकारे त्याची ऑक्सिडेशन स्थिती -1 आहे.
 3 कृपया लक्षात घ्या की मेटल आयनमध्ये अनेक ऑक्सिडेशन अवस्था असू शकतात. अनेक धातू घटकांचे अणू वेगवेगळ्या प्रमाणात आयनीकरण करू शकतात. उदाहरणार्थ, लोह (Fe) सारख्या धातूचा आयन चार्ज +2 किंवा +3 असतो. धातूच्या आयन (आणि त्यांची ऑक्सिडेशन स्थिती) चा चार्ज इतर घटकांच्या आयनच्या शुल्काद्वारे निर्धारित केला जाऊ शकतो ज्यासह हा धातू रासायनिक संयुगाचा भाग आहे; मजकुरामध्ये, हे शुल्क रोमन अंकांद्वारे दर्शविले जाते: उदाहरणार्थ, लोह (III) ची ऑक्सिडेशन स्थिती +3 आहे.
3 कृपया लक्षात घ्या की मेटल आयनमध्ये अनेक ऑक्सिडेशन अवस्था असू शकतात. अनेक धातू घटकांचे अणू वेगवेगळ्या प्रमाणात आयनीकरण करू शकतात. उदाहरणार्थ, लोह (Fe) सारख्या धातूचा आयन चार्ज +2 किंवा +3 असतो. धातूच्या आयन (आणि त्यांची ऑक्सिडेशन स्थिती) चा चार्ज इतर घटकांच्या आयनच्या शुल्काद्वारे निर्धारित केला जाऊ शकतो ज्यासह हा धातू रासायनिक संयुगाचा भाग आहे; मजकुरामध्ये, हे शुल्क रोमन अंकांद्वारे दर्शविले जाते: उदाहरणार्थ, लोह (III) ची ऑक्सिडेशन स्थिती +3 आहे. - उदाहरण म्हणून, अॅल्युमिनियम आयन असलेल्या कंपाऊंडचा विचार करा. AlCl कंपाऊंडचा एकूण शुल्क3 शून्य आहे.आम्हाला माहित आहे की Cl आयनचे शुल्क -1 आहे, आणि कंपाऊंडमध्ये 3 असे आयन आहेत, प्रश्नातील पदार्थाच्या सामान्य तटस्थतेसाठी, अल आयनला +3 चा चार्ज असणे आवश्यक आहे. अशा प्रकारे, या प्रकरणात, अॅल्युमिनियमची ऑक्सिडेशन स्थिती +3 आहे.
 4 ऑक्सिजनची ऑक्सिडेशन स्थिती -2 आहे (काही अपवाद वगळता). जवळजवळ सर्व प्रकरणांमध्ये, ऑक्सिजन अणूंची ऑक्सिडेशन स्थिती -2 असते. या नियमाला अनेक अपवाद आहेत:
4 ऑक्सिजनची ऑक्सिडेशन स्थिती -2 आहे (काही अपवाद वगळता). जवळजवळ सर्व प्रकरणांमध्ये, ऑक्सिजन अणूंची ऑक्सिडेशन स्थिती -2 असते. या नियमाला अनेक अपवाद आहेत: - जर ऑक्सिजन मूलभूत अवस्थेत असेल (ओ2), त्याची ऑक्सिडेशन स्थिती 0 आहे, जसे इतर प्राथमिक पदार्थांच्या बाबतीत.
- ऑक्सिजनचा भाग असल्यास पेरोक्साइड, त्याची ऑक्सिडेशन स्थिती -1 आहे. पेरोक्साइड हे संयुगांचा समूह आहे ज्यात एक साधा ऑक्सिजन-ऑक्सिजन बंध असतो (म्हणजे पेरोक्साइड आयन ओ2). उदाहरणार्थ, एच च्या रचना मध्ये2ओ2 (हायड्रोजन पेरोक्साइड) ऑक्सिजनची चार्ज आणि ऑक्सिडेशन स्थिती -1 असते.
- फ्लोरीनसह एकत्र केल्यावर, ऑक्सिजनची ऑक्सिडेशन स्थिती +2 असते, खाली फ्लोरीनसाठी नियम वाचा.
 5 हायड्रोजनमध्ये काही अपवाद वगळता +1 ची ऑक्सिडेशन स्थिती असते. ऑक्सिजन प्रमाणे, अपवाद देखील आहेत. नियमानुसार, हायड्रोजनची ऑक्सिडेशन स्थिती +1 आहे (जर ती मूलभूत स्थिती H मध्ये नसेल तर2). तथापि, हायड्राइड नावाच्या संयुगांमध्ये, हायड्रोजनची ऑक्सिडेशन स्थिती -1 आहे.
5 हायड्रोजनमध्ये काही अपवाद वगळता +1 ची ऑक्सिडेशन स्थिती असते. ऑक्सिजन प्रमाणे, अपवाद देखील आहेत. नियमानुसार, हायड्रोजनची ऑक्सिडेशन स्थिती +1 आहे (जर ती मूलभूत स्थिती H मध्ये नसेल तर2). तथापि, हायड्राइड नावाच्या संयुगांमध्ये, हायड्रोजनची ऑक्सिडेशन स्थिती -1 आहे. - उदाहरणार्थ, एच मध्ये2O हायड्रोजनची ऑक्सिडेशन स्थिती +1 आहे कारण ऑक्सिजन अणूवर -2 चा चार्ज असतो आणि एकूण तटस्थतेसाठी दोन +1 शुल्क आवश्यक असतात. तरीसुद्धा, सोडियम हायड्राइडच्या रचनेत, हायड्रोजनची ऑक्सिडेशन अवस्था आधीच -1 आहे, कारण ना आयन +1 चा भार घेते, आणि सामान्य इलेक्ट्रोन्यूट्रॅलिटीसाठी, हायड्रोजन अणूचा (आणि अशाप्रकारे त्याची ऑक्सिडेशन स्थिती) चार्ज असावा -1 असा.
 6 फ्लोरीन नेहमी -1 ची ऑक्सिडेशन स्थिती आहे. आधीच नमूद केल्याप्रमाणे, काही घटकांची ऑक्सिडेशन स्थिती (धातूचे आयन, पेरोक्साईडमधील ऑक्सिजन अणू, इत्यादी) अनेक घटकांवर अवलंबून बदलू शकतात. फ्लोरीनची ऑक्सिडेशन स्थिती मात्र नेहमी -1 असते. हे या घटकामध्ये सर्वात जास्त इलेक्ट्रोनगेटिव्हिटी आहे या वस्तुस्थितीमुळे आहे - दुसऱ्या शब्दांत, फ्लोरीन अणू त्यांच्या स्वत: च्या इलेक्ट्रॉनसह भाग घेण्यास कमीत कमी इच्छुक असतात आणि परदेशी इलेक्ट्रॉनला सक्रियपणे आकर्षित करतात. अशा प्रकारे, त्यांचे शुल्क अपरिवर्तित राहते.
6 फ्लोरीन नेहमी -1 ची ऑक्सिडेशन स्थिती आहे. आधीच नमूद केल्याप्रमाणे, काही घटकांची ऑक्सिडेशन स्थिती (धातूचे आयन, पेरोक्साईडमधील ऑक्सिजन अणू, इत्यादी) अनेक घटकांवर अवलंबून बदलू शकतात. फ्लोरीनची ऑक्सिडेशन स्थिती मात्र नेहमी -1 असते. हे या घटकामध्ये सर्वात जास्त इलेक्ट्रोनगेटिव्हिटी आहे या वस्तुस्थितीमुळे आहे - दुसऱ्या शब्दांत, फ्लोरीन अणू त्यांच्या स्वत: च्या इलेक्ट्रॉनसह भाग घेण्यास कमीत कमी इच्छुक असतात आणि परदेशी इलेक्ट्रॉनला सक्रियपणे आकर्षित करतात. अशा प्रकारे, त्यांचे शुल्क अपरिवर्तित राहते.  7 कंपाऊंडमधील ऑक्सिडेशन स्टेट्सची बेरीज त्याच्या चार्जच्या बरोबरीची आहे. रासायनिक कंपाऊंड बनवणाऱ्या सर्व अणूंची ऑक्सिडेशन अवस्था या कंपाऊंडच्या शुल्कामध्ये जोडली पाहिजे. उदाहरणार्थ, जर कंपाऊंड तटस्थ असेल तर त्याच्या सर्व अणूंच्या ऑक्सिडेशन स्टेट्सची बेरीज शून्य असावी; जर कंपाऊंड -1 च्या शुल्कासह पॉलीआटोमिक आयन असेल तर ऑक्सिडेशन स्टेट्सची बेरीज -1 आहे, आणि असेच.
7 कंपाऊंडमधील ऑक्सिडेशन स्टेट्सची बेरीज त्याच्या चार्जच्या बरोबरीची आहे. रासायनिक कंपाऊंड बनवणाऱ्या सर्व अणूंची ऑक्सिडेशन अवस्था या कंपाऊंडच्या शुल्कामध्ये जोडली पाहिजे. उदाहरणार्थ, जर कंपाऊंड तटस्थ असेल तर त्याच्या सर्व अणूंच्या ऑक्सिडेशन स्टेट्सची बेरीज शून्य असावी; जर कंपाऊंड -1 च्या शुल्कासह पॉलीआटोमिक आयन असेल तर ऑक्सिडेशन स्टेट्सची बेरीज -1 आहे, आणि असेच. - ही एक चांगली चाचणी पद्धत आहे - जर ऑक्सिडेशन राज्यांची बेरीज कंपाऊंडच्या एकूण शुल्काची बरोबरी करत नसेल, तर तुम्ही कुठेतरी चुकीचे आहात.
भाग 2 मधील 2: रसायनशास्त्राचे नियम न वापरता ऑक्सिडेशन स्थिती निश्चित करणे
 1 त्यांच्या अक्सिडेशन स्थितीबद्दल कठोर नियम नसलेले अणू शोधा. काही घटकांसाठी, ऑक्सिडेशन स्थिती शोधण्यासाठी कोणतेही दृढपणे स्थापित केलेले नियम नाहीत. जर अणू वर सूचीबद्ध केलेल्या कोणत्याही नियमांमध्ये बसत नसेल आणि आपल्याला त्याचे शुल्क माहित नसेल (उदाहरणार्थ, अणू एका कॉम्प्लेक्सचा भाग आहे आणि त्याचे शुल्क निर्दिष्ट केलेले नाही), आपण अशा अणूची ऑक्सिडेशन स्थिती निर्धारित करू शकता बहिष्काराने. प्रथम, कंपाऊंडमधील इतर सर्व अणूंचे शुल्क निश्चित करा आणि नंतर, कंपाऊंडच्या ज्ञात एकूण शुल्कावरून, या अणूच्या ऑक्सिडेशन स्थितीची गणना करा.
1 त्यांच्या अक्सिडेशन स्थितीबद्दल कठोर नियम नसलेले अणू शोधा. काही घटकांसाठी, ऑक्सिडेशन स्थिती शोधण्यासाठी कोणतेही दृढपणे स्थापित केलेले नियम नाहीत. जर अणू वर सूचीबद्ध केलेल्या कोणत्याही नियमांमध्ये बसत नसेल आणि आपल्याला त्याचे शुल्क माहित नसेल (उदाहरणार्थ, अणू एका कॉम्प्लेक्सचा भाग आहे आणि त्याचे शुल्क निर्दिष्ट केलेले नाही), आपण अशा अणूची ऑक्सिडेशन स्थिती निर्धारित करू शकता बहिष्काराने. प्रथम, कंपाऊंडमधील इतर सर्व अणूंचे शुल्क निश्चित करा आणि नंतर, कंपाऊंडच्या ज्ञात एकूण शुल्कावरून, या अणूच्या ऑक्सिडेशन स्थितीची गणना करा. - उदाहरणार्थ, कंपाऊंडमध्ये Na2SO4 सल्फर अणूचा चार्ज अज्ञात आहे - आम्हाला फक्त माहित आहे की ते शून्य नाही, कारण सल्फर प्राथमिक अवस्थेत नाही. हे कंपाऊंड ऑक्सिडेशन स्थिती निश्चित करण्यासाठी बीजगणित पद्धत स्पष्ट करण्यासाठी एक चांगले उदाहरण म्हणून काम करते.
 2 कंपाऊंडमधील उर्वरित घटकांची ऑक्सिडेशन अवस्था शोधा. वर वर्णन केलेल्या नियमांचा वापर करून, कंपाऊंडच्या उर्वरित अणूंची ऑक्सिडेशन अवस्था निश्चित करा. O, H वगैरे नियमांना अपवाद विसरू नका.
2 कंपाऊंडमधील उर्वरित घटकांची ऑक्सिडेशन अवस्था शोधा. वर वर्णन केलेल्या नियमांचा वापर करून, कंपाऊंडच्या उर्वरित अणूंची ऑक्सिडेशन अवस्था निश्चित करा. O, H वगैरे नियमांना अपवाद विसरू नका. - Na साठी2SO4, आमचे नियम वापरून, आम्हाला आढळले की Na आयनचे शुल्क (आणि म्हणून ऑक्सिडेशन स्थिती) +1 आहे आणि प्रत्येक ऑक्सिजन अणूंसाठी ते -2 आहे.
 3 अणूंची संख्या त्यांच्या ऑक्सिडेशन स्थितीनुसार गुणाकार करा. आता आपल्याला एक वगळता सर्व अणूंची ऑक्सिडेशन अवस्था माहित आहे, हे लक्षात घेणे आवश्यक आहे की काही घटकांचे अनेक अणू असू शकतात. प्रत्येक घटकाच्या अणूंची संख्या (ते घटकाच्या चिन्हाच्या अनुषंगाने सबस्क्रिप्ट म्हणून कंपाऊंडच्या रासायनिक सूत्रात दर्शविले जाते) त्याच्या ऑक्सिडेशन स्थितीद्वारे गुणाकार करा.
3 अणूंची संख्या त्यांच्या ऑक्सिडेशन स्थितीनुसार गुणाकार करा. आता आपल्याला एक वगळता सर्व अणूंची ऑक्सिडेशन अवस्था माहित आहे, हे लक्षात घेणे आवश्यक आहे की काही घटकांचे अनेक अणू असू शकतात. प्रत्येक घटकाच्या अणूंची संख्या (ते घटकाच्या चिन्हाच्या अनुषंगाने सबस्क्रिप्ट म्हणून कंपाऊंडच्या रासायनिक सूत्रात दर्शविले जाते) त्याच्या ऑक्सिडेशन स्थितीद्वारे गुणाकार करा. - Na मध्ये2SO4 आपल्याकडे 2 Na अणू आणि 4 O अणू आहेत. अशा प्रकारे, 2 × +1 गुणा केल्यावर, आम्हाला सर्व Na अणूंची ऑक्सिडेशन स्थिती मिळते (2), आणि 4 × -2 -O (-8) अणूंची ऑक्सिडेशन स्थिती मिळवते.
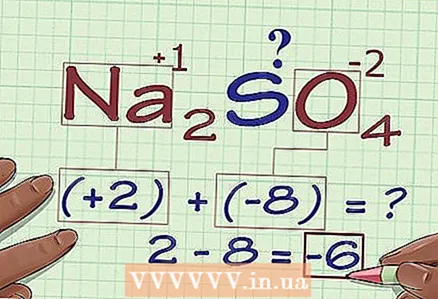 4 मागील निकाल जोडा. गुणाकारांच्या परिणामांचा सारांश, आम्हाला कंपाऊंडची ऑक्सिडेशन स्थिती मिळते शिवाय इच्छित अणूचे योगदान लक्षात घेऊन.
4 मागील निकाल जोडा. गुणाकारांच्या परिणामांचा सारांश, आम्हाला कंपाऊंडची ऑक्सिडेशन स्थिती मिळते शिवाय इच्छित अणूचे योगदान लक्षात घेऊन. - आमच्या उदाहरणात, Na साठी2SO4 आम्ही 2 आणि -8 जोडतो आणि -6 मिळवतो.
 5 कंपाऊंडच्या चार्जमधून अज्ञात ऑक्सिडेशन स्थिती शोधा. आपल्याकडे आता इच्छित ऑक्सिडेशन स्थितीची सहज गणना करण्यासाठी सर्व डेटा आहे. डावीकडे एक समीकरण लिहा, ज्याच्या मागील गणना पायरीमध्ये प्राप्त झालेल्या संख्येची बेरीज आणि अज्ञात ऑक्सिडेशन स्थिती असेल आणि कंपाऊंडच्या एकूण शुल्काच्या उजव्या बाजूला असेल. दुसऱ्या शब्दात, (ज्ञात ऑक्सिडेशन स्टेट्सची बेरीज) + (इच्छित ऑक्सिडेशन स्टेट) = (कंपाऊंडचा चार्ज).
5 कंपाऊंडच्या चार्जमधून अज्ञात ऑक्सिडेशन स्थिती शोधा. आपल्याकडे आता इच्छित ऑक्सिडेशन स्थितीची सहज गणना करण्यासाठी सर्व डेटा आहे. डावीकडे एक समीकरण लिहा, ज्याच्या मागील गणना पायरीमध्ये प्राप्त झालेल्या संख्येची बेरीज आणि अज्ञात ऑक्सिडेशन स्थिती असेल आणि कंपाऊंडच्या एकूण शुल्काच्या उजव्या बाजूला असेल. दुसऱ्या शब्दात, (ज्ञात ऑक्सिडेशन स्टेट्सची बेरीज) + (इच्छित ऑक्सिडेशन स्टेट) = (कंपाऊंडचा चार्ज).- आमच्या बाबतीत, ना2SO4 उपाय असे दिसते:
- (ज्ञात ऑक्सिडेशन स्टेट्सची बेरीज) + (इच्छित ऑक्सिडेशन स्टेट) = (कंपाऊंड चार्ज)
- -6 + एस = 0
- एस = 0 + 6
- S = 6.V Na2SO4 सल्फरची ऑक्सिडेशन स्थिती असते 6.
- आमच्या बाबतीत, ना2SO4 उपाय असे दिसते:
टिपा
- संयुगांमध्ये, सर्व ऑक्सिडेशन राज्यांची बेरीज शुल्क समान असणे आवश्यक आहे. उदाहरणार्थ, जर कंपाऊंड डायटॉमिक आयन असेल तर अणूंच्या ऑक्सिडेशन स्टेट्सची बेरीज एकूण आयनिक चार्जच्या बरोबरीची असणे आवश्यक आहे.
- आवर्त सारणी वापरण्यास सक्षम असणे आणि त्यात धातू आणि धातू नसलेले घटक कोठे आहेत हे जाणून घेणे खूप उपयुक्त आहे.
- प्राथमिक स्वरूपात अणूंची ऑक्सिडेशन स्थिती नेहमी शून्य असते. एकाच आयनची ऑक्सिडेशन स्थिती त्याच्या चार्जच्या बरोबरीची असते. नियतकालिक सारणीच्या गट 1 ए मधील घटक, जसे की हायड्रोजन, लिथियम, सोडियम, मूलभूत स्वरूपात +1 ची ऑक्सिडेशन स्थिती असते; गट 2 ए धातूंची ऑक्सिडेशन स्थिती, जसे मॅग्नेशियम आणि कॅल्शियम, मूलभूत स्वरूपात +2 आहे. ऑक्सिजन आणि हायड्रोजन, रासायनिक बंधाच्या प्रकारानुसार, 2 भिन्न ऑक्सिडेशन अवस्था असू शकतात.
आपल्याला काय आवश्यक आहे
- घटकांची आवर्त सारणी
- इंटरनेट प्रवेश किंवा रसायनशास्त्र संदर्भ पुस्तके
- कागद, पेन किंवा पेन्सिलची शीट
- कॅल्क्युलेटर