लेखक:
Robert Simon
निर्मितीची तारीख:
24 जून 2021
अद्यतन तारीख:
1 जुलै 2024

सामग्री
- पाऊल टाकण्यासाठी
- भाग 1 चा 1: मर्यादित अभिकर्मक निश्चित करणे
- भाग २ चा भाग: सैद्धांतिक उत्पन्न निश्चित करणे
सैद्धांतिक उत्पन्न म्हणजे रासायनिक अभिक्रियाकडून आपण अपेक्षित असलेल्या जास्तीत जास्त पदार्थासाठी रसायनशास्त्र वापरले जाते. आपण प्रतिक्रियेचे समीकरण संतुलित करून आणि मर्यादित अभिकर्मक परिभाषित करता. आपण वापरू इच्छित रीएजेंटची मात्रा मोजता तेव्हा आपण प्राप्त केलेल्या पदार्थाची मात्रा मोजू शकता. हे समीकरणांचे सैद्धांतिक उत्पन्न आहे. वास्तविक प्रयोगात, आपण कदाचित त्यातील काही गमवाल, कारण हा एक आदर्श प्रयोग नाही.
पाऊल टाकण्यासाठी
भाग 1 चा 1: मर्यादित अभिकर्मक निश्चित करणे
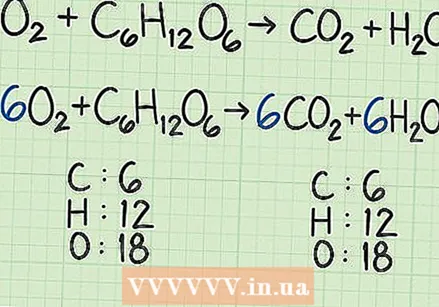 समतोल प्रतिक्रियेसह प्रारंभ करा. प्रतिक्रिया समीकरण रेसिपीसारखेच आहे. हे दर्शवते की कोणती अभिक्रेजे (डावीकडील) उत्पादने तयार करण्यासाठी एकमेकांशी प्रतिक्रिया करतात (उजवीकडे). समतोल प्रतिक्रियेमध्ये समीकरणाच्या डाव्या बाजूला (अणुभट्ट्या म्हणून) उजवीकडील (उत्पादनांच्या स्वरूपात) अणूंची समान संख्या असते.
समतोल प्रतिक्रियेसह प्रारंभ करा. प्रतिक्रिया समीकरण रेसिपीसारखेच आहे. हे दर्शवते की कोणती अभिक्रेजे (डावीकडील) उत्पादने तयार करण्यासाठी एकमेकांशी प्रतिक्रिया करतात (उजवीकडे). समतोल प्रतिक्रियेमध्ये समीकरणाच्या डाव्या बाजूला (अणुभट्ट्या म्हणून) उजवीकडील (उत्पादनांच्या स्वरूपात) अणूंची समान संख्या असते. - उदाहरणार्थ, समजू की आपल्याकडे साधे समीकरण आहे
 प्रत्येक प्रतिक्रियेच्या मोलर मासांची गणना करा. नियतकालिक सारणी किंवा इतर काही संदर्भ पुस्तक वापरुन प्रत्येक रचनेतील प्रत्येक अणूचा दाढीचा समूह शोधा. अभिकर्मकांच्या प्रत्येक कंपाऊंडचे दाढर द्रव्य शोधण्यासाठी त्यांना एकत्र जोडा. कंपाऊंडच्या एकाच रेणूसाठी हे करा. ऑक्सिजन आणि ग्लूकोजचे कार्बन डाय ऑक्साईड आणि पाण्यात रूपांतर करण्याचे समीकरण पुन्हा विचारात घ्या:
प्रत्येक प्रतिक्रियेच्या मोलर मासांची गणना करा. नियतकालिक सारणी किंवा इतर काही संदर्भ पुस्तक वापरुन प्रत्येक रचनेतील प्रत्येक अणूचा दाढीचा समूह शोधा. अभिकर्मकांच्या प्रत्येक कंपाऊंडचे दाढर द्रव्य शोधण्यासाठी त्यांना एकत्र जोडा. कंपाऊंडच्या एकाच रेणूसाठी हे करा. ऑक्सिजन आणि ग्लूकोजचे कार्बन डाय ऑक्साईड आणि पाण्यात रूपांतर करण्याचे समीकरण पुन्हा विचारात घ्या: 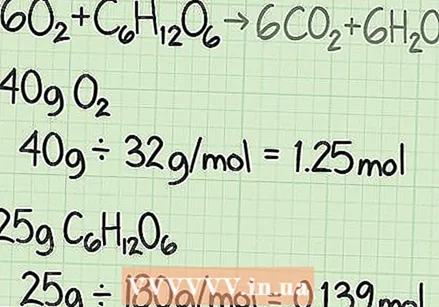 प्रत्येक अभिकर्मकांचे प्रमाण ग्रॅम ते मोल्समध्ये रूपांतरित करा. वास्तविक प्रयोगासाठी, आपण वापरत असलेल्या प्रत्येक अभिकर्मकांच्या ग्रॅममधील वस्तुमान ज्ञात होतील. हे मूल्य मोलच्या संख्येमध्ये रूपांतरित करताना त्या पदार्थाच्या मोलर मासद्वारे विभाजित करा.
प्रत्येक अभिकर्मकांचे प्रमाण ग्रॅम ते मोल्समध्ये रूपांतरित करा. वास्तविक प्रयोगासाठी, आपण वापरत असलेल्या प्रत्येक अभिकर्मकांच्या ग्रॅममधील वस्तुमान ज्ञात होतील. हे मूल्य मोलच्या संख्येमध्ये रूपांतरित करताना त्या पदार्थाच्या मोलर मासद्वारे विभाजित करा. - उदाहरणार्थ, समजा आपण 40 ग्रॅम ऑक्सिजन आणि 25 ग्रॅम ग्लूकोजसह प्रारंभ करता.
- 40 ग्रॅम
 अभिकर्मकांचा दातांचे प्रमाण निश्चित करा. तीळ हे मोजण्याचे एक साधन आहे जे त्यांच्या वस्तुमानावर आधारित रेणू मोजण्यासाठी रसायनशास्त्रात वापरले जाते. ऑक्सिजन आणि ग्लूकोज या दोहोंच्या मॉल्सची संख्या ठरवून आपल्याला माहित आहे की आपण किती अणूपासून प्रारंभ करता. दोहोंचे प्रमाण शोधण्यासाठी, एका अभिकर्मकाच्या मोल्सची संख्या दुसर्याच्या भागाद्वारे विभाजित करा.
अभिकर्मकांचा दातांचे प्रमाण निश्चित करा. तीळ हे मोजण्याचे एक साधन आहे जे त्यांच्या वस्तुमानावर आधारित रेणू मोजण्यासाठी रसायनशास्त्रात वापरले जाते. ऑक्सिजन आणि ग्लूकोज या दोहोंच्या मॉल्सची संख्या ठरवून आपल्याला माहित आहे की आपण किती अणूपासून प्रारंभ करता. दोहोंचे प्रमाण शोधण्यासाठी, एका अभिकर्मकाच्या मोल्सची संख्या दुसर्याच्या भागाद्वारे विभाजित करा. - खालील उदाहरणात, आपण ऑक्सिजनच्या 1.25 मोल्स आणि ग्लूकोजच्या 0.139 मोल्सपासून प्रारंभ करा. तर ऑक्सिजन आणि ग्लूकोज रेणूंचे प्रमाण 1.25 / 0.139 = 9.0 आहे. या प्रमाणानुसार आपल्याकडे ग्लूकोजपेक्षा ऑक्सिजनचे नऊपट रेणू आहेत.
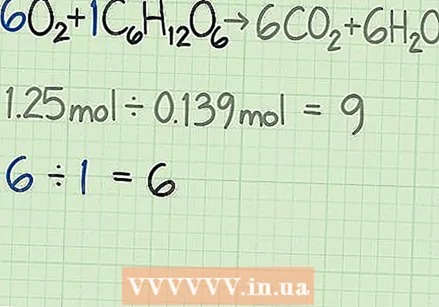 प्रतिक्रियेसाठी आदर्श प्रमाण निश्चित करा. समतोल प्रतिसाद पहा. प्रत्येक रेणूचे गुणांक आपल्याला प्रतिक्रिया देण्यासाठी आवश्यक असलेल्या रेणूंचे गुणोत्तर सांगतात. जर आपण सूत्राद्वारे दिले गेलेले गुणोत्तर वापरत असाल तर दोन्ही अभिकर्मक समान प्रमाणात वापरले पाहिजेत.
प्रतिक्रियेसाठी आदर्श प्रमाण निश्चित करा. समतोल प्रतिसाद पहा. प्रत्येक रेणूचे गुणांक आपल्याला प्रतिक्रिया देण्यासाठी आवश्यक असलेल्या रेणूंचे गुणोत्तर सांगतात. जर आपण सूत्राद्वारे दिले गेलेले गुणोत्तर वापरत असाल तर दोन्ही अभिकर्मक समान प्रमाणात वापरले पाहिजेत. - या प्रतिक्रियेसाठी अणुभट्ट्यांना दिले गेले आहेत
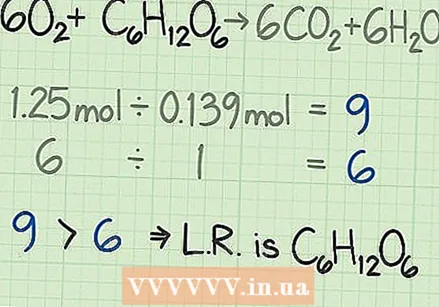 मर्यादित अभिकर्मक शोधण्यासाठी प्रमाण तुलना करा. बहुतेक रासायनिक अभिक्रियांमध्ये, अभिकर्मकांपैकी एक आधीच्यापेक्षा पूर्वी वापरला जाईल. आधी वापरल्या जाणार्या रीएजेंटला मर्यादीत अभिकर्मक म्हणतात. हे मर्यादीत अभिकर्मक हे निर्धारित करते की रासायनिक प्रतिक्रिया किती काळ चालू राहू शकते आणि सैद्धांतिक उत्पन्नाची आपण अपेक्षा करू शकता. मर्यादित अभिकर्मक निश्चित करण्यासाठी आपण मोजलेल्या दोन गुणोत्तरांची तुलना करा:
मर्यादित अभिकर्मक शोधण्यासाठी प्रमाण तुलना करा. बहुतेक रासायनिक अभिक्रियांमध्ये, अभिकर्मकांपैकी एक आधीच्यापेक्षा पूर्वी वापरला जाईल. आधी वापरल्या जाणार्या रीएजेंटला मर्यादीत अभिकर्मक म्हणतात. हे मर्यादीत अभिकर्मक हे निर्धारित करते की रासायनिक प्रतिक्रिया किती काळ चालू राहू शकते आणि सैद्धांतिक उत्पन्नाची आपण अपेक्षा करू शकता. मर्यादित अभिकर्मक निश्चित करण्यासाठी आपण मोजलेल्या दोन गुणोत्तरांची तुलना करा: - खालील उदाहरणात, आपण मोल द्वारे मोजलेल्या ग्लूकोजपेक्षा नऊ पट ऑक्सिजनसह प्रारंभ करा. सूत्र आपल्याला सांगते की आपले आदर्श प्रमाण ग्लूकोजपेक्षा सहापट जास्त ऑक्सिजन आहे. तर आपल्याला ग्लूकोजपेक्षा जास्त ऑक्सिजनची आवश्यकता आहे. तर दुसरा अभिकर्मक, या प्रकरणात ग्लूकोज मर्यादित अभिकर्मक आहे.
- या प्रतिक्रियेसाठी अणुभट्ट्यांना दिले गेले आहेत
- उदाहरणार्थ, समजू की आपल्याकडे साधे समीकरण आहे
भाग २ चा भाग: सैद्धांतिक उत्पन्न निश्चित करणे
 आपल्याला पाहिजे असलेले उत्पादन शोधण्यासाठी प्रतिसाद पहा. रासायनिक समीकरणाची उजवी बाजू प्रतिक्रीयाचे उत्पादन दर्शवते. जेव्हा प्रतिक्रिया संतुलित केली जाते, तेव्हा प्रत्येक उत्पादनाचे गुणांक सूचित करतात की आपण किती आण्विक प्रमाणांची अपेक्षा करू शकता. प्रत्येक उत्पादनाचे एक सैद्धांतिक उत्पन्न असते किंवा जेव्हा प्रतिक्रिया पूर्ण होते तेव्हा आपण अपेक्षा करता त्या उत्पादनाचे प्रमाण.
आपल्याला पाहिजे असलेले उत्पादन शोधण्यासाठी प्रतिसाद पहा. रासायनिक समीकरणाची उजवी बाजू प्रतिक्रीयाचे उत्पादन दर्शवते. जेव्हा प्रतिक्रिया संतुलित केली जाते, तेव्हा प्रत्येक उत्पादनाचे गुणांक सूचित करतात की आपण किती आण्विक प्रमाणांची अपेक्षा करू शकता. प्रत्येक उत्पादनाचे एक सैद्धांतिक उत्पन्न असते किंवा जेव्हा प्रतिक्रिया पूर्ण होते तेव्हा आपण अपेक्षा करता त्या उत्पादनाचे प्रमाण. - वरील उदाहरणासह पुढे जाणे, आपण प्रतिसादाचे विश्लेषण करता
 आपल्या मर्यादित अभिकर्मकाच्या मोल्सची संख्या नोंदवा. आपण नेहमी उत्पादनाच्या मोलांच्या संख्येसह मर्यादित अभिकर्मकांच्या मोलांच्या संख्येची तुलना केली पाहिजे. आपण प्रत्येकाच्या वस्तुमानांची तुलना करण्याचा प्रयत्न केल्यास आपल्याला योग्य निकाल मिळणार नाही.
आपल्या मर्यादित अभिकर्मकाच्या मोल्सची संख्या नोंदवा. आपण नेहमी उत्पादनाच्या मोलांच्या संख्येसह मर्यादित अभिकर्मकांच्या मोलांच्या संख्येची तुलना केली पाहिजे. आपण प्रत्येकाच्या वस्तुमानांची तुलना करण्याचा प्रयत्न केल्यास आपल्याला योग्य निकाल मिळणार नाही. - वरील उदाहरणात, ग्लूकोज मर्यादित अभिकर्मक आहे. मोलार मास गणनानुसार ग्लूकोजचे पहिले 25 ग्रॅम ग्लूकोजच्या 0.139 मोल इतके असते.
 उत्पादनातील रेणू आणि अभिकर्मक यांच्यातील गुणोत्तरांची तुलना करा. समतोल प्रतिक्रियेकडे परत या. आपल्या मर्यादित अभिकर्मकाच्या रेणूंच्या संख्येनुसार आपल्या इच्छित उत्पादनाचे रेणूंची संख्या विभाजित करा.
उत्पादनातील रेणू आणि अभिकर्मक यांच्यातील गुणोत्तरांची तुलना करा. समतोल प्रतिक्रियेकडे परत या. आपल्या मर्यादित अभिकर्मकाच्या रेणूंच्या संख्येनुसार आपल्या इच्छित उत्पादनाचे रेणूंची संख्या विभाजित करा. - या उदाहरणासाठी समतोल प्रतिक्रिया आहे
 मर्यादित अभिकर्मकाच्या मोल्सच्या संख्येने हे गुणोत्तर गुणाकार करा. उत्तर इच्छित उत्पादनांचे सैद्धांतिक उत्पन्न आहे.
मर्यादित अभिकर्मकाच्या मोल्सच्या संख्येने हे गुणोत्तर गुणाकार करा. उत्तर इच्छित उत्पादनांचे सैद्धांतिक उत्पन्न आहे. - या उदाहरणात, ग्लूकोजचे 25 ग्रॅम ग्लूकोजच्या 0.139 मोल्सच्या बरोबरीचे आहे. कार्बन डाय ऑक्साईड आणि ग्लूकोजचे प्रमाण 6: 1 आहे. आपण प्रारंभ केला आहे की आपण सुरू केलेल्या ग्लूकोजच्या मोलांच्या संख्येपेक्षा कार्बन डाय ऑक्साईडच्या तब्बल सहापट उत्पादन करण्यास सक्षम असाल.
- कार्बन डाय ऑक्साईडचे सैद्धांतिक उत्पन्न (0.139 मोल ग्लूकोज) एक्स (6 मोल कार्बन डाय ऑक्साईड / मोल ग्लूकोज) = 0.834 मोल कार्बन डाय ऑक्साईड आहे.
 निकाल ग्रॅममध्ये रुपांतरित करा. हे मोल्सची संख्या किंवा रीएजेंटची रक्कम मोजण्याच्या आपल्या मागील चरणातील उलट आहे. जेव्हा आपण अपेक्षा करू शकत असलेल्या मोल्सची संख्या आपल्याला ठाऊक असेल, तर उत्पादनातील मोलरच्या प्रमाणात ते गुणामध्ये सैद्धांतिक उत्पन्न शोधण्यासाठी गुणाकार करा.
निकाल ग्रॅममध्ये रुपांतरित करा. हे मोल्सची संख्या किंवा रीएजेंटची रक्कम मोजण्याच्या आपल्या मागील चरणातील उलट आहे. जेव्हा आपण अपेक्षा करू शकत असलेल्या मोल्सची संख्या आपल्याला ठाऊक असेल, तर उत्पादनातील मोलरच्या प्रमाणात ते गुणामध्ये सैद्धांतिक उत्पन्न शोधण्यासाठी गुणाकार करा. - पुढील उदाहरणात सीओचा मोलार मास आहे2 सुमारे 44 ग्रॅम / मोल. (कार्बनचे मोलार द्रव्यमान ~ 12 ग्रॅम / मोल आणि ऑक्सिजन ~ 16 ग्रॅम / मोल आहे, म्हणून एकूण 12 + 16 + 16 = 44 आहे).
- सीओचे 0.834 मोल गुणा करा2 x 44 ग्रॅम / मोल सीओ2 = ~ 36.7 ग्रॅम. प्रयोगाचे सैद्धांतिक उत्पन्न 36.7 ग्रॅम सीओ आहे2.
 इच्छित असल्यास इतर उत्पादनांसाठी गणना पुन्हा करा. बर्याच प्रयोगांमध्ये आपल्याला कदाचित एखाद्या विशिष्ट उत्पादनाच्या उत्पन्नामध्ये रस असेल. आपण दोन्ही उत्पादनांचे सैद्धांतिक उत्पन्न जाणून घेऊ इच्छित असल्यास, आपल्याला प्रक्रिया पुन्हा करायची आहे.
इच्छित असल्यास इतर उत्पादनांसाठी गणना पुन्हा करा. बर्याच प्रयोगांमध्ये आपल्याला कदाचित एखाद्या विशिष्ट उत्पादनाच्या उत्पन्नामध्ये रस असेल. आपण दोन्ही उत्पादनांचे सैद्धांतिक उत्पन्न जाणून घेऊ इच्छित असल्यास, आपल्याला प्रक्रिया पुन्हा करायची आहे. - या उदाहरणात पाणी हे दुसरे उत्पादन आहे
. समतोल प्रतिक्रियेनुसार आपण ग्लूकोजच्या एका रेणूमधून पाण्याचे सहा रेणूंची अपेक्षा करू शकता. हे प्रमाण 6: 1 आहे. तर ग्लूकोजच्या 0.139 मोल्स पाण्यात 0.834 मोल असावेत.
- पाण्याचे दाणेदार द्रव्यमान पाण्यातील मोल्सची संख्या गुणाकार करा. मोलार द्रव्यमान 2 + 16 = 18 ग्रॅम / मोल आहे. उत्पादनाद्वारे गुणाकार, याचा परिणाम 0.139 मोल एच2ओ x 18 ग्रॅम / मोल एच2ओ = ~ 2.50 ग्रॅम. या प्रयोगातील पाण्याचे सैद्धांतिक उत्पन्न 2.50 ग्रॅम आहे.
- या उदाहरणात पाणी हे दुसरे उत्पादन आहे
- या उदाहरणासाठी समतोल प्रतिक्रिया आहे
- वरील उदाहरणासह पुढे जाणे, आपण प्रतिसादाचे विश्लेषण करता